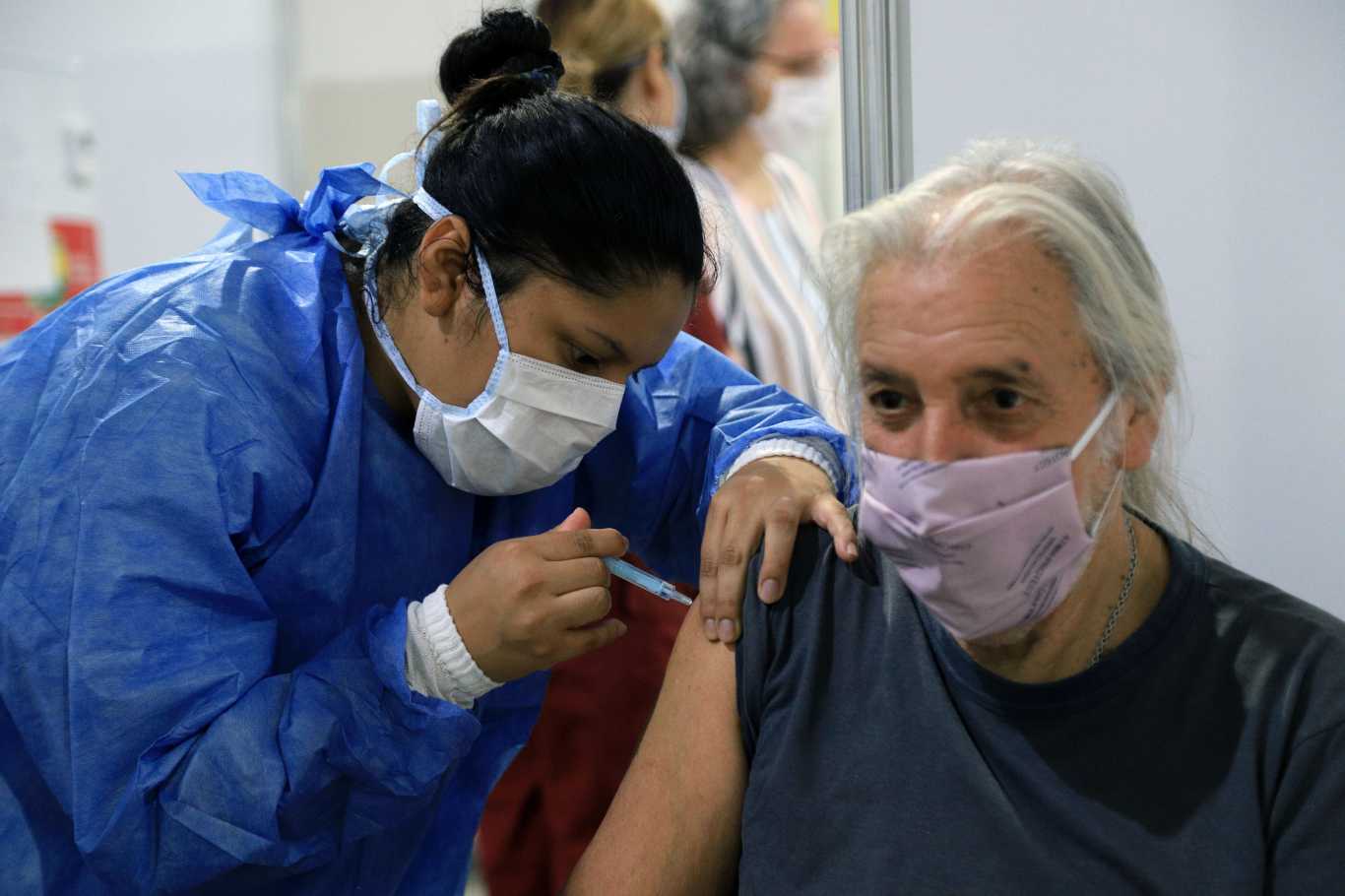
SALTA (Redacción) – La OMS recomendó una tercera dosis para grupos de riesgo. La organización propuso que la vacunación contra el coronavirus, se la indique una vez más a las personas con «sistema inmunológico grave o moderadamente comprometido». El mexicano Alejandro Cravioto, presidente del Grupo Asesor Estratégico de Expertos de la OMS, fue quien hizo este anuncio.
La determinación se tomó luego de la reunión que se realizó la semana pasada, donde se analizaron las estrategias de vacunación contra la Covid-19 y otras enfermedades. Sobre la tercera dosis (o segunda en el caso de la vacuna monodosis de Johnson & Johnson), en principio debe administrarse a personas con un «sistema inmunológico grave o moderadamente comprometido».

El experto mexicano Cravioto aclaró que esta recomendación se aplica a todas las vacunas que la OMS ha aprobado para su uso de emergencia contra la Covid-19, como Pfizer-BioNTech, Moderna, AstraZeneca, Johnson & Johnson, Sinopharm y Sinovac. En los próximos días seguramente se unirá la del laboratorio indio Bharat, según adelantó el profesional.
La dosis de refuerzo puede ser de otra vacuna de otro tipo a la del esquema recibido en un primer momento, precisó el Grupo Estratégico Consultivo de Expertos (SAGE) de la OMS, en una rueda de prensa. La luz verde a una tercera dosis, limitada a ciertos colectivos, se produce después de que en agosto la OMS pidiera no administrar dosis de refuerzo hasta finales de septiembre.
Píldora contra el coronavirus
Se trata de «un medicamento antiviral oral en fase de investigación para el tratamiento del covid-19 de leve a moderado en adultos que corren el riesgo de evolucionar a covid-19 grave y/o de ser hospitalizados». La empresa farmacéutica Merck informó este lunes que solicitó a las autoridades sanitarias de los Estados Unidos la autorización para el uso de emergencia de su medicamento.
La empresa señaló que «si se autoriza, Molnupiravir podría ser el primer medicamento antiviral oral para el tratamiento de covid-19”. Se trata de «un medicamento antiviral oral en fase de investigación para el tratamiento del covid-19 de leve a moderado en adultos que corren el riesgo de evolucionar a covid-19 grave y/o de ser hospitalizados».
El medicamento fue probado en 170 países, entre ellos la Argentina. Ahora Merck espera que la aprobación de la FDA para poder venderlo, mientras aguarda también que otras agencias reguladoras también autorice su uso. De esta manera, se abre un nuevo camino para el tratamiento del coronavirus que va más allá de las vacunas.